

发布时间:2026-04-07
近日,中国科学院广州生物医药与健康研究院联合美国约翰霍普金斯大学、国科大杭州高等研究院在PNAS发表题为Structure-guided design of 7-azaindole DNMT1 inhibitors active against hypomethylating agent–resistant acute myeloid leukemia的研究论文。该研究开发出一类以7-氮杂吲哚为核心骨架的新型DNMT1选择性抑制剂。代表性化合物DMI46在去甲基化药物耐药急性髓系白血病(AML)模型中表现出显著抗肿瘤活性与良好安全性,为难治性AML药物研发提供潜在候选分子。
启动子区域DNA过度甲基化可导致关键抑癌基因表达沉默,从而驱动恶性肿瘤发生与进展。抑制DNA甲基转移酶DNMT1、逆转异常甲基化并恢复抑癌基因表达,已成为肿瘤治疗的重要策略。当前,核苷类去甲基化药物地西他滨和阿扎胞苷虽已获批用于AML等血液肿瘤一线治疗,但其作用依赖掺入DNA并诱导DNMT1形成高细胞毒性的DNA-蛋白交联物,进而引发显著DNA损伤与剂量限制性毒性。受此限制,现有去甲基化药物的临床响应率仅约为40%,且大多数初始有效患者在两年内出现获得性耐药,预后不佳。因此,开发毒性更低、能够克服核苷类去甲基化药物耐药的新型DNMT1抑制剂具有重要临床价值。
研究团队前期发现,DNMT1催化结构域在“开放-关闭”两种构象间的动态转换是其发挥甲基化活性的前提(ACS Chem Biol, 2018),为开发通过阻断构象转换实现抑制效应的非核苷类DNMT1抑制剂提供理论依据。本研究围绕该构象调控关键区域,采用基于结构的骨架跃迁与药物化学优化策略,并结合自主建立的高灵敏细胞水平甲基化抑制剂筛选体系(Adv Sci, 2026),设计获得新型7-氮杂吲哚类DNMT1抑制剂。代表性化合物DMI46可有效重塑肿瘤细胞异常高甲基化状态,重新激活抑癌基因表达并发挥显著抗AML活性。与临床药物地西他滨相比,DMI46无需掺入DNA,不引起明显DNA损伤,且对正常造血细胞毒性更低,显示出更优安全性和更宽治疗窗口。
进一步的冷冻电镜结构分析显示,7-氮杂吲哚骨架不仅与DNMT1形成关键相互作用,还与DNA产生更强的π-π堆积效应,使化合物稳定“锚定”于DNMT1/DNA复合物中,并促进其苯环取代基向催化loop和DNA识别螺旋区延伸,最终将DNMT1锁定在持续开放的非活性构象,从而阻断其催化所需的构象转换。重要的是,这种强“锚定”效应可转化为更稳定、持久的DNMT1在靶抑制作用,使DMI46在体内外均能有效抑制对既有非核苷类DNMT1抑制剂及临床药物地西他滨耐药的AML疾病进展。
化学干预 DNA 甲基化不仅可作用于肿瘤细胞,也可调控免疫细胞与造血细胞的命运决定,故具有广泛的转化应用潜力。本研究开发的新型DNMT1抑制剂除有望用于耐药AML治疗外,还可进一步拓展至基于化学重编程的免疫细胞治疗,以及与免疫检查点抑制剂联用以协同增强抗实体瘤效果。此外,研究团队近期还与复旦大学蓝贤江教授合作发现,在我国广东、广西地区高发的遗传性疾病β-地中海贫血模型中,DMI46可选择性诱导胎儿血红蛋白去甲基化并激活表达,重塑红细胞命运并促进其成熟,从而延缓β-地中海贫血症进展(Adv Sci, 2025),进一步表明此类化合物在华南地区高发遗传性疾病治疗中的重要应用前景。
广州健康院唐士兵研究员、博士生宗梁怡、尚依妮(现为中山大学博士生),以及杭高院马舒元(现为哈尔滨工业大学博士生)、博士生魏家乐为论文共同第一作者。广州健康院孔祥谦研究员、唐士兵研究员,美国约翰霍普金斯大学Stephen Baylin教授和杭高院李智海研究员为论文共同通讯作者。该研究还得到上海药物研究所罗成研究员,广州健康院陈奇研究员、潘光锦研究员、朱艳玲副研究员、黄靖副研究员,浙江理工大学叶飞教授和广州国家实验室翁桁游研究员的大力支持,并获得科技部重点研发计划、中国科学院战略性先导科技专项、广州健康院抢占科技制高点重大项目和广州国家实验室重大研究计划等项目资助。
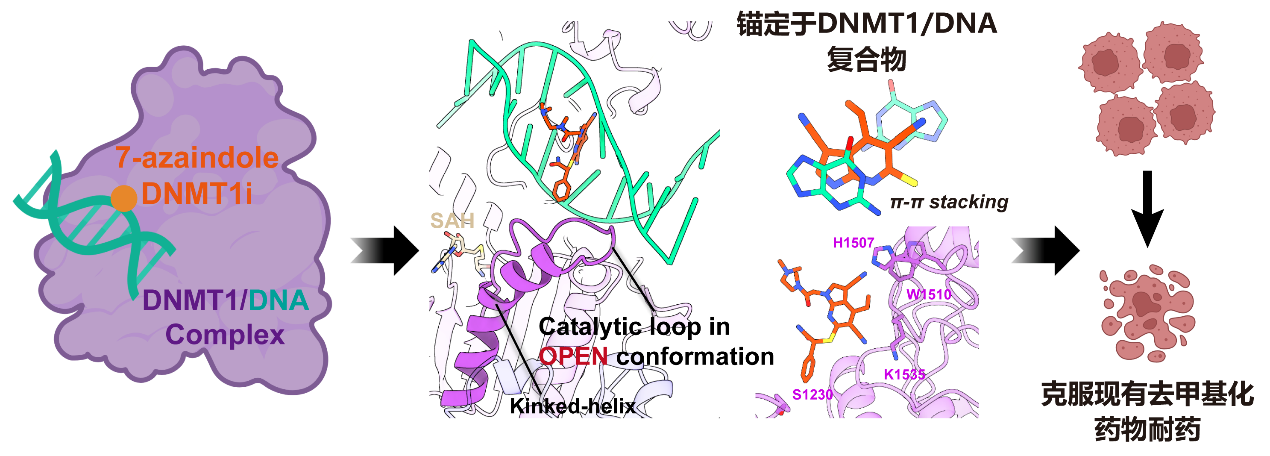
图1. DMI46通过将DNMT1锁定于持续开放构象,有效克服现有DNA去甲基化药物耐药
附件下载:



