

发布时间:2026-04-07
2026年4月3日,中国科学院广州生物医药与健康研究院细胞器与干细胞研究组与多单位合作在SCIENCE CHINA Life Sciences发表题为A new role of Iridium(III) Complexes in regulating pluripotency acquisition via mitochondrial remodulation的论文。该研究独辟蹊径,将金属有机化学与干细胞生物学、肿瘤学深度交叉,首次发现类原本用于抗癌的铱(III)配合物,作为新型线粒体靶向分子,通过调控线粒体分布与表观遗传修饰, 快速打开体细胞“重返青春”为诱导多能干细胞(iPS)的大门;同时调控肿瘤干细胞干性。该研究不仅揭示了铱(III)配合物调控线粒体-细胞核之间的信号交流的全新模式,而且为小分子化合物诱导细胞命运提供了“金属离子”的新思路。
铱在现代医学尤其是肿瘤领域的应用日益广泛,其中铱(III)配合物作为新型抗癌分子,兼具强效抗癌活性与低毒性优势。研究团队聚焦体细胞重编程与肿瘤干细胞调控两大核心方向,系统开展了铱(III)配合物的功能与机制研究。在体细胞重编程领域,研究发现铱(III)配合物可显著提升小鼠体细胞向iPSCs的诱导效率,其核心作用靶点为线粒体:该配合物可特异性诱导线粒体向细胞核周围聚集,缩短线粒体与细胞核的信号传递距离,增强线粒体-核通讯效率;同时促进线粒体TCA循环酶Pdha1的核转位,驱动细胞代谢从氧化磷酸化向糖酵解转换——这一代谢特征与多能干细胞的能量代谢模式高度契合,可显著增加乙酰辅酶A的生成量,为组蛋白乙酰化修饰提供充足底物。
进一步机制解析表明,铱(III)配合物诱导的Pdha1核转位的核心效应事件:通过Pdha1核转位与代谢重编程的协同作用,显著提升组蛋白H3K9、H3K27等关键位点的乙酰化水平,重塑多能性基因位点的染色质状态,促进Oct4、Sox2等核心多能性基因的转录激活,最终实现体细胞向多能干细胞的高效转换。
同时,研究团队意外发现铱(III)配合物具有上下文依赖的双重生物学功能:在肿瘤干细胞中,该配合物通过线粒体靶向作用诱导线粒体活性氧(ROS)高浓度累积,破坏线粒体动力学平衡,抑制肿瘤干细胞的自我更新能力与致瘤性;而在正常体细胞中,其诱导的低浓度ROS作为信号分子,可进一步促进线粒体核周分布与Pdha1核转位,协同提升重编程效率。这种“促再生-抑癌”双重功能,为再生医学与癌症联合治疗提供了全新的分子工具。
该研究阐明的“铱(III)配合物-线粒体核周分布-Pdha1核转位-代谢-表观遗传重塑”调控通路,是一种全新的细胞命运调控模式,不仅丰富了线粒体反向信号调控的理论体系,为金属配合物在再生医学中开辟了新路径,而且拓展了铱(III)配合物的生物学功能边界,建立了金属配合物作为小分子化合物诱导细胞分化的全新范式。其次,该研究也为肿瘤干细胞靶向治疗难等关键科学问题提供了新靶点与新思路,其“促重编程-抑癌”双重功能,有望开发为兼具组织修复与肿瘤治疗的多功能制剂,为癌症治疗后组织再生提供新策略。再次,铱作为一种在地质历史上与恐龙灭绝事件相关的稀有元素,其在表观遗传调控中的新发现也为地球生命演化研究提供了有趣的联想。
本研究是中国科学院广州生物医药健康研究院、广州医科大学、中山大学、中国科学院香港创新研究院再生医学与健康创新中心等多个研究组合作完成。本研究获国家自然科学基金、国家重点研发项目、中国科学院、广东省、广州市等的经费支持。中国科学院广州生物医药健康研究院刘兴国研究员、广州医科大学龙琪教授为本论文的共同通讯作者。中国科学院广州生物医药健康研究院吴昊、李伟为本文共同第一作者。
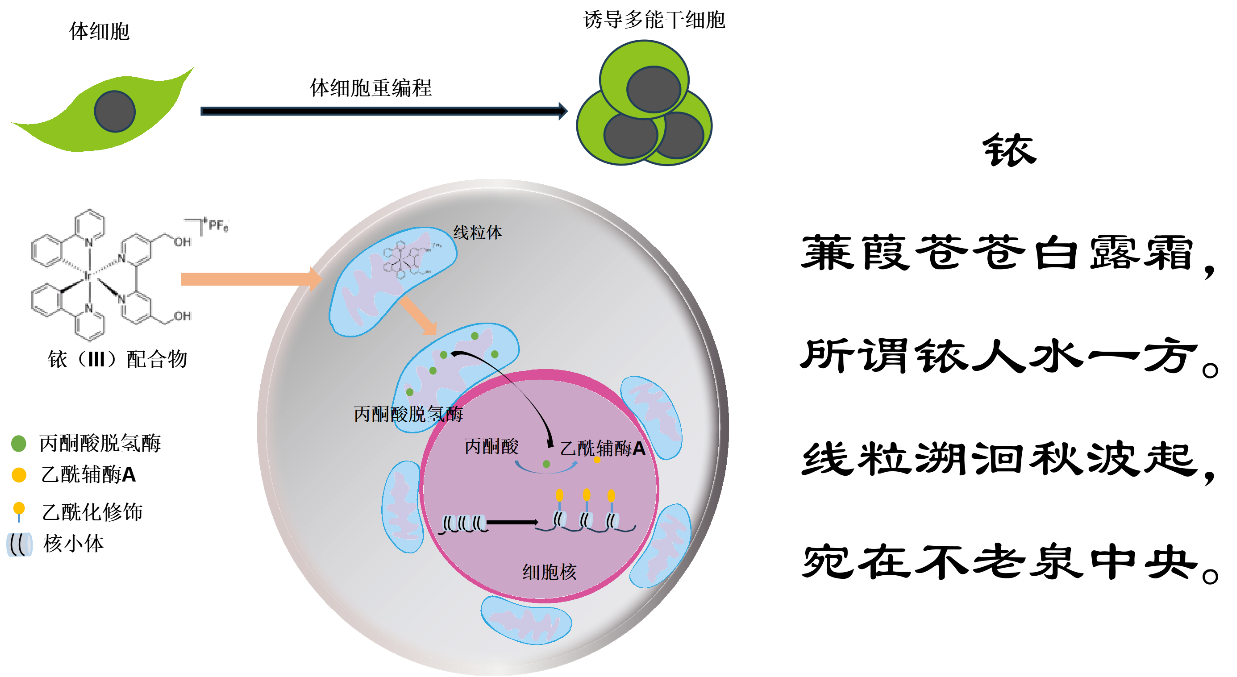
图注:铱(III)配合物通过调控线粒体分布与表观遗传修饰调控多能性。铱(III)配合物与线粒体的奇妙羁绊,正是“蒹葭苍苍白露霜,所谓铱人水一方”,所谓“铱人”便是靶向线粒体的铱(III)配合物,隔着细胞质的“秋水”,与细胞核遥遥相望;“线粒溯洄秋波起”,铱(III)配合物诱导线粒体核周聚集“溯洄”,都是向细胞核传递调控信号的暗送秋波;这一调控机制最终唤醒体细胞的多能性潜能,让细胞重获“不老”的再生活力,正是“宛在不老泉中央”。——来自刘兴国研究员的创意
附件下载:



