

发布时间:2016-04-25来源:来源:《广东科技报》
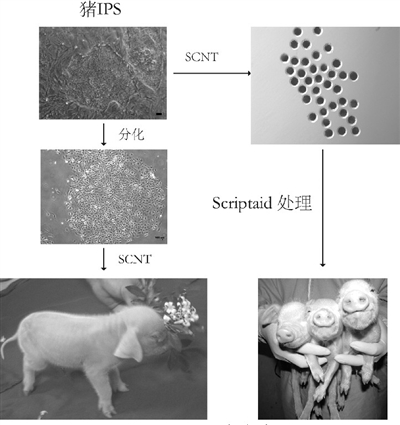
iPS克隆猪

研究团队成员合影
本报记者 张建列 通讯员 黄博纯
世界上首次获得了iPS克隆猪,为基于iPS进行基因修饰大动物的制作打通了技术路线;首次将锌指核酸酶介导的基因打靶技术应用于猪基因修饰,使猪体细胞打靶效率由10-6提高到4%,实现了对大动物高效基因打靶;首次将2A序列介导的多基因转移技术应用于猪基因组修饰,成功获得了四色荧光猪,并实现了多个外源基因在动物体内的高效协同表达……这些原创成果出自中国科学院广州生物医药与健康研究院联合南方医科大学、浙江大学、深圳华大基因研究院等完成的项目《猪基因突变技术创新及基因修饰猪模型的建立》,该项目组在大动物基因修饰技术方面所取得的突破及所获得的动物模型,将进一步促进基因修饰大动物作为生物医药模型的研究,推动生物医药业的发展,并由此获2015年度广东省科学技术奖一等奖。
猪是更理想的人类疾病模型
人类疾病动物模型作为人类疾病的“复制品”,可按研究者的需要随时采集各种样品或分批处死动物收集标本,以了解疾病全过程,这是临床难以办到的。项目的第二完成人、中国科学院广州生物医药与健康研究院副研究员樊娜娜介绍,人类疾病的动物模型是指各种医学科学研究中建立的具有人类疾病模拟表现的动物,包括小鼠、猪、狗等,主要用于实验生理学、实验病理学和实验治疗学(包括新药筛选)研究。“与人类完全相同的动物自发性疾病模型毕竟不可多得,往往需要人工加以复制。为了尽量做到与人类疾病相似,首先要注意动物的选择。”
从基因角度上看,猪与人类基因的相似性达到83%,因此猪在医学研究上有很大前景。樊娜娜说,小鼠与人在心血管系统、神经系统、营养代谢等方面与人体差异较大,用做人类疾病模型时不能准确反映人类疾病;小鼠体型小、寿命短不适合进行一些治疗技术开发和长效研究。“比如,因为猪与人类生理比较接近,我们可以让猪得人类的疾病,进而探讨治疗方法,这比将小鼠作为模型动物要可靠得多。
“小鼠研究模型有很多种,也很成熟,但和人的差异比较大,不能完全反映人的情况。炎症反应小鼠和人是不同的,前几年美国曾经上市一种治疗糖尿病的药品,在小鼠实验的效果非常理想,然而用到人身上却副作用非常大,最终这个药被撤了。现在美国FDA审批药物上临床治疗时,要求有大动物模型实验后,才能用到人上。”
获得世界首例iPS克隆猪
猪的生理特征、器官组织结构和人类比较类似,特别是猪的肝脏、心脏等器官与人类的相似性也很高,科学家们一直在寻找将猪作为人源化器官培养体的方式。樊娜娜说,这一切都需要制备基因修饰猪。自2007年起,在项目的第一完成人、中国科学院广州生物医药与健康研究院研究员赖良学的带领下,项目组聚焦大动物基因修饰技术研究及基因修饰动物模型的建立工作。
樊娜娜介绍:“目前来说转基因猪制备包括随机转基因和基因打靶两种方式,其中:随机转基因猪是把外源基因放到猪里面,让猪表达它自己没有的基因;基因打靶是把某个基因放到猪基因的特定位置,想对猪的哪个基因进行突变或修饰都可以。基因打靶包括两种功能:一是基因敲除,即把某个基因去掉,二是基因敲入,是把某个基因放到基因组的某一个地方。”
但是,由于缺乏猪胚胎干细胞,转基因猪的制备主要依赖于体细胞基因修饰和体细胞核移植技术。这种技术用来进行随机转基因猪的制作无压力,但是由于体细胞打靶效率极低,对猪进行基因定点修饰非常困难。这成了研究中最大的瓶颈。各国科学家都希望通过猪的iPS(诱导多能干细胞,induced pluripotent stem cells)来克隆猪,但未能获成功。“iPS的出现为大动物基因打靶提供了新的希望。获得基因打靶的iPS细胞之后,一方面可以通过嵌合体技术,获得生殖系嵌合的动物,经过交配获得基因修饰动物;另一方面,可将这些基因打靶iPS细胞为核供体,通过核移植技术获得基因修饰克隆动物。”
在不懈努力下,项目组发现外源基因的表达和表观遗传学可能是影响iPS克隆胚胎发育的主要原因,经过反复的实验,项目组在2011年获得世界上第一个成活的iPS克隆猪。iPS来源克隆猪的成功,为基于iPS 进行基因修饰猪的制作打通了技术路线。克服了以体细胞进行基因修饰存在的体外增殖能力有限,打靶效率低的难题。
大动物领域,基因打靶技术国际领先
如何提升猪的打靶效率?樊娜娜表示,“以前大动物上没有胚胎干细胞(ES),体细胞打靶效率极低,在小鼠上能做的东西大动物上做不到,或者说能做但很难做,所以我们做不过啮齿类动物。但是近十年,随着锌指核酸酶基因打靶技术、TALENs基因敲除技术、CRISPR/Cas9基因敲除技术等兴起,这几种新的基因打靶技术的出现使大动物的基因定向修饰变得非常容易,通过这几种技术现在我们可以在大动物上实现基因打靶了。”
2008年,锌指核酸酶基因打靶技术被开发出来,“当时我们项目组立即跟进,将该技术应用于猪胎儿成纤维细胞进行基因打靶,使体细胞打靶效率由10-6 提高到4%;确立了以锌指核酸酶基因打靶技术对胎儿成纤维进行打靶后再进行核移植的高效基因打靶猪制作技术路线。樊娜娜坦言,获奖项目只是针对锌指核酸酶基因打靶技术的应用,但是项目组一直没有停步,一直紧跟基因打靶技术的前沿,在TALENs基因敲除技术和CRISPR/Cas9基因敲除技术等当前先进基因修饰技术在大动物基因修饰应用领域,项目组也处于国际的领先水平。
“目前来说,国内外在转基因、基因打靶方面技术基本上与国际是同步的,但这些技术都不是我们国内科学家发现的,而把这些技术应用到大动物领域并取得重大研究成果我们是占据了领先位置。”
促进猪模型在生物医药的应用研究
据悉,通过实施该项目,项目组在Cell Research、Human Molecular Genetics等杂志上发表论文5篇,其中发表在Human Molecular Genetics的论文被选为封面文章刊出。论文被SCI数据库论文总引用149次,他引115次,单篇最高引用49次,他引42次。项目在大动物基因修饰技术方面所取得的突破及所获得的动物模型将进一步促进基因修饰大动物作为生物医药模型的研究,推动生物医药业的发展,具有巨大的社会效益和经济效益。
“目前,我们建立了多种人类疾病模型猪、器官移植模型猪、基础研究工具猪模型等。其中,我们建立的人类亨廷顿疾病模型猪表现出与人类亨廷顿舞蹈症患者脑中类似的神经细胞凋亡现象,这在亨廷顿疾病模型中是首次见到。”樊娜娜解析说,亨廷顿疾病是遗传性神经退行性疾病,影响肌肉的协调性,导致认知功能减退和精神问题。猪的大脑结构与人更为接近,适合用于人退行性神经疾病的研究。“亨廷顿疾病模型猪已列入亨廷顿疾病协作组,对全世界亨廷顿疾病研究团队开放使用,以促进亨廷顿疾病治疗研究,《猪基因突变技术创新及基因修饰猪模型的建立》项目的完成推动了我国大动物模型研究工作,促进了猪这一大动物模型在生物医药领域的应用研究。”
樊娜娜也坦言,这些人类疾病模型猪还处于发展的初期。目前,这些模型做出来了但是还没有得到大规模的应用,这里有多方面的原因:一是没有相应的高标准的饲养条件,如无病原饲养室,如免疫缺陷型模型猪对病源无抵抗力,在普通饲养环境中不能长期存活;另外,对猪行为学、影像学的研究缺少完善的评价体系,导致很多模型无法广泛应用,这些评价标准还需要实验动物行为学的专业人员参与制定。
基因修饰猪应用未来大有前途
猪作为重要的经济动物是人类生活关系最为密切的家畜之一,转基因猪在农业领域中应用广泛。可以对猪的基因进行改造,提高猪肉产量,改善猪肉的质量,增加猪肉的营养价值等,也可以提高猪的抗病能力。樊娜娜还举了一个例子,比如糖尿病人,是不能吃糖的。“但是可以将一种糖味蛋白基因转到牛身上,让这个基因在乳腺中表达,那么这种牛产出的奶就是有甜味。这种牛奶的甜味不是来自糖而是来自蛋白,这样糖尿病人就可以吃到有甜味的牛奶了。”
猪在解剖、组织、生理和营养代谢等方面均与人类最接近,在生物医药方面,可以进行异种器官移植,即把猪的器官移植到人身上,比如把猪的肾脏、心脏、胰脏、角膜等往人身上移。在此之前,赖良学研究员及其合作者曾经将超级性排斥相关基因敲除后的猪心脏移植到狒狒身上,并成功最终存活了6个月左右。樊娜娜说,猪器官移植到人体,阻碍异种器官移植工作获得成功的首要问题是免疫学上的排异反应问题,再就是猪的内源性病毒。“猪的内源性病毒是整合在猪的基因组内的,对猪是没有影响,但是猪器官移植到人体,病毒可能会被激活,让人感染得病。目前我们项目组正在把这些病毒基因敲掉。”
目前干细胞技术发展很快,更大胆的展望是人源化器官的实现,“让猪体内长出人的器官。”樊娜娜解释说,将来把人的干细胞放到器官缺陷猪的早期胚胎中,这样猪就可以长出人的器官,这就是人源化器官,在此之前有日本科学家在小鼠身上长出大鼠的胰脏,说明人源化器官的预想是可实现的,这也是未来大有前途的研究领域。在赖良学研究员的带领下,项目组目前已经在开展人源化器官的研究工作。
来源:《广东科技报》4月22日特别报道
附件下载:



